-
-
静脉血栓栓塞症(venous thromboembolism, VTE)是下肢深静脉血栓(deep vein thrombosis, DVT)和肺栓塞(pulmonary embolus, PE)的统称。VTE被认为是目前临床上的常见疾病, 尽管我国的发病率至今尚无数据统计, 然在美国大约每年至少有25万新发病例[1]。
抗凝治疗在VTE治疗中的地位已无可质疑。伴随着美国胸科医师协会(American College of Chest Physicians, ACCP)关于VTE预防和治疗指南(第8版[2]和第9版[3])在国内的推广, 对于有罹患VTE高危因素的患者, 如骨关节置换术后[4]、多发性外伤[5]等, 积极地使用抗凝药物进行预防已深入人心。同样, 对于已经罹患VTE的患者, 由血管外科医生为主进行积极的抗凝药物治疗也逐渐推广并规范化。尽早诊断, 第一时间治疗以及足量有效的药物治疗理念正逐渐为临床医生所接受, 我国关于DVT和PE诊断和治疗的指南也已纷纷出台[6-7]。
至今, 抗凝的主要药物仍然是肝素类药物和口服维生素K拮抗剂(vitamin K antagonist, VKA)。1914年, 医学生Jay Mclean首次发现了肝素, 并首次在上世纪40年代用于临床。50年代, VKA也首次被运用于临床抗凝治疗。低分子肝素(low molecular weight heparin, LMWH)被用于临床也已经超过20年。肝素类药物和VKA治疗, 除了可用于VTE治疗外; 还用于高危患者VTE的预防, 有血栓栓塞事件高危心房颤动患者、冠状动脉腔内治疗围术期、动脉手术中以及外周动脉重建术后预防再闭塞病例。
肝素和VKA类药物已被广泛使用, 其安全性和有效性已得到学术界的认可, 但迄今为止, 这些药物仍有一些问题无法解决, 尤其是VKA的问题更多一些。VKA起效时间慢, 治疗窗口相对较窄, 需要严格的实验室检测国际标准化比值(international normalized ratio, INR), 而且INR结果受其他药物、食物交叉影响较多, 对于依从性差的病例操作有一定的风险。至于普通肝素和LMWH, 需要通过静脉或皮下注射治疗, 门诊操作不够简便。同时, 肝素诱导性血小板减少症(heparin induced thrombocytopenia, HIT)也是肝素类药物罕见但是严重的不良反应。
上述问题提示, VTE患者非常需要一种更加安全可靠、方便的抗凝药物。这种药物应该具备以下特点:更广的治疗适应证、相对简单的药代动力学和药物相互作用, 最好口服使用, 而目前在研的3种药物(利伐沙班、达比加群酯和阿哌沙班)无疑已走在了研究的前列, 成为近2年来学术界所关注的新药物。这些新药都直接作用于凝血过程的单一靶点(Ⅱa或Ⅹa因子), 而VKA与多个位点凝血因子相关, 是3种新药与VKA类药物作用机制完全不同之处。本文围绕上述3种药物的研究进展, 描述VTE治疗和预防前景, 同时也介绍一些其他药物的研究进展。
阿哌沙班
阿哌沙班(apixaban)是一种Ⅹa因子直接抑制剂(同时阻断内源性和外源性凝血途径)。口服药物的生物利用度超过50%, 3~4 h后血浆药物浓度达峰值, 半衰期10~14 h, 体内代谢受CYP3A4影响, 肾脏排泄25%[8-9]。阿哌沙班不与肝药酶CYP3A4发生抑制或促进作用, 所以与其他药物的相互作用很少。另外, 由于阿哌沙班为肝肾双通道代谢, 故轻-中度肝肾功能损害患者也可以安全使用。
阿哌沙班Ⅱ期试验提示其用于预防和治疗VTE的药物剂量窗口较宽[10]。第1个Ⅲ期临床研究是关于骨关节术后预防VTE的研究(ADVANCE-1)[11], 该研究共纳入3195例患者, 为随机双盲研究, 入组患者在术后12~24 h开始预防性抗凝治疗, 随机服用阿哌沙班(2.5 mg、2次/d)或依诺肝素(30 mg皮下注射1次/12 h), 术后2周进行静脉造影监测, 主要观察终点是VTE(症状性或造影发现)及全因死亡。结果两组主要观察终点接近(阿哌沙班组8.99%, 依诺肝素组8.85%), 终点事件发生率相近及阿哌沙班组的出血率显著减少, 提示阿哌沙班是1种有效的抗凝药物。ADVANCE-2研究[12], 是1个全球多中心研究, 针对全膝关节置换术后, 随机双盲对照阿哌沙班(2.5 mg、2次/d)和依诺肝素(40 mg皮下注射1次/d)抗凝效果。主要观察终点是所有VTE事件, 结果阿哌沙班组发生率为15.1%, 依诺肝素组为24.4%(RR=0.62, P < 0.001), 两组出血事件发生率比较差异虽无统计学意义, 但阿哌沙班组出血发生率还是低于依诺肝素组(3.2%和4.8%, P=0.09)。
用于治疗急性VTE(DVT+PE)的3期临床研究AMPLIFY试验无疑最受国内血管外科医生关注, 阿哌沙班组治疗前7 d剂量为10 mg、2次/d, 其后6个月每天5 mg、2次/d; 对照组为依诺肝素+VKA治疗。AMPLIFY试验目前已经完成受试者招募工作, 我国也有20多家医院参加。另外, 其后的3期延长试验将针对已经口服抗凝药物6个月的VTE患者, 观察是否需要继续抗凝治疗, 试验将患者随机分为3组, 分别为安慰剂、阿哌沙班2.5 mg (2次/d)及阿哌沙班5 mg(2次/d)组。两个试验的主要观察终点是复发性VTE或死亡, 这些结果均值得拭目以待。
阿哌沙班目前在欧盟29个国家获得批准上市, 用于骨科术后VTE预防, 被第9版ACCP指南推荐可以用于骨科术后预防, 证据级别1B[13]。
达比加群酯
达比加群酯(dabigatran etexilate)直接抑制游离凝血酶和血栓结合的凝血酶。经口服的达比加群酯在肝代谢中迅速转化为达比加群, 血浆药物浓度1.5 h可以达峰值, 稳定期半衰期为15~17 h, 口服生物利用度为7.2%, 未吸收的达比加群酯主要经粪便排泄[14]。尽管部分达比加群酯生物转化过程在肝内进行, 但并不涉及P450系统。达比加群酯主要与奎尼丁类和维拉帕米类药物发生相互作用。经肝激活后的达比加群主要经肾脏(80%以上)排泄, 所以建议对轻-中度肾功能不全患者减量使用, 而对重度肾功能不全患者禁忌使用。
有3个大规模达比加群酯3期临床试验对骨关节手术后VTE的预防作用进行验证。RE-NOVATE试验[15]随机分为3组, 分别为达比加群酯220 mg(1次/d)、150 mg(1次/d)和依诺肝素40 mg(1次/d)组, 主要观察终点是VTE和全因死亡。结果两组达比加群酯的预防作用均不比依诺肝素差, 主要出血事件也与依诺肝素相当, 220 mg组为2.0%(P=0.44)、150 mg组为1.3%(P=0.6)、依诺肝素组为1.6%。RE-MODEL试验[16]为全膝关节术后VTE预防研究, 主要观察终点为VTE和全因死亡, 达比加群酯220 mg组为36.4%、150 mg组为40.5%、依诺肝素组为37.7%。这2个试验均证明达比加群酯对VTE的预防作用不比依诺肝素差。RE-MOBILIZE试验[17]的依诺肝素为30 mg、2次/d, 结果达比加群酯220 mg组总体观察事件为31.1%、150 mg组为33.7%、依诺肝素组为25.3%, 提示达比加群酯在全膝关节术后的预防作用可能不如北美标准剂量的依诺肝素抗凝方案(2次/d), 但与欧洲常用预防剂量效果相当(1次/d)。
目前, VTE的治疗研究包括:RE-COVER-1[18]在29个国家的228个中心完成, 共入组2564例患者。试验设计为随机双盲双模拟对照, 达比加群组150 mg、2次/d, 对照组采用依诺肝素+华法林治疗, 总治疗时间6个月, 观察病例均为急性(15 d内)VTE患者, 观察终点为复发VTE和全因死亡。结果达比加群组血栓复发率为2.4%, 而对照组为2.1%, HR=1.10, 95%CI 0.65~1.84;达比加群组大出血发生率为1.6%, 对照组为1.9%, HR=0.82, 95%CI 0.45~1.48;达比加群组总体出血率为16.1%, 对照组为21.9%, HR=0.71, 95%CI 0.59~0.85(P < 0.05)。RECOVER-2试验[19]也在2011年完成, 通过扩大的样本人群获得的结果同样证明达比加群与华法林预防VTE复发的作用相当。另外, 用于研究更长期抗凝治疗的RE-SONATE试验[20], 观察人群是已经规律华法林治疗VTE患者停药后的二级预防, 试验发现, 相对于安慰剂, 达比加群可以降低92%的VTE远期复发事件。目前达比加群已经在欧洲、加拿大等40个国家获准为骨科手术后VTE预防适应证, 另有美国等40个国家批准其用于预防心房颤动导致的卒中。在2012出版的第9版ACCP中, 被推荐使用于骨科手术后VTE预防, 证据级别1B[13]。
利伐沙班
利伐沙班(rivaroxaban)也是1种Ⅹa因子直接抑制剂, 口服后3 h达峰值, 稳定的药物半衰期4~9 h(大于75岁可能为12 h)。很少发生药物和食物相互作用, 口服生物利用度可以达到80%[21]。与阿哌沙班相近, 利伐沙班也同时抑制游离和结合的Ⅹ因子。66%的药物经肾脏代谢, 其余通过胆汁代谢。目前对于肌酐清除率小于30 ml/min的病例, 禁忌使用利伐沙班。另外, 对于轻-中度肾功能不全患者使用利伐沙班也需小心, 目前尚无相关的剂量调整方案。
在4项RECORD(1-4)试验中[22-25], 利伐沙班10 mg(1次/d)组比依诺肝素组预防VTE更有优势。4个试验共有超过12 000例患者入组, 但利伐沙班组出血率较高, 为0.39%, 而依诺肝素组为0.21%(P=0.08);大出血发生率, 利伐沙班组为1.80%, 依诺肝素组为1.37%(P=0.06)。
利伐沙班用于治疗急性VTE的3期药物试验是同类产品中最早完成的。EINSTEIN-DVT[26]和EINSTEIN-PE试验[27]分别对3449例DVT患者和4836例PE患者进行开放标签、随机对照试验。利伐沙班组前3周15 mg、2次/d, 其后改为20 mg、1次/d; 对照组为依诺肝素+VKA。抗凝时间根据患者血栓危险因素分为3、6和12个月。这2项试验我国也有多家中心参加。EINSTEIN-DVT试验发现, 利伐沙班治疗急性DVT患者的效果不劣于传统低分子肝素+华法林治疗。利伐沙班组主要终点事件(血栓复发+全因死亡)为36例(2.1%), 对照组51例(3.0%), 危险比0.68(95%CI 0.44%~1.04%), 两组主要安全性事件均为8.1%。EINSTEIN-PE试验发现, 对急性PE患者两种药物的主要终点事件也没有统计学差异, 研究药物组和对照组分别为2.1%和1.8%, 危险比为1.12(95%CI 0.75%~1.68%); 两组大出血发生率分别为1.1%和2.2%, 危险比0.49(95%CI 0.31%~0.79%, P=0.003), 利伐沙班体现了一定的优势。还有一项二级预防研究[26, 28], 入选病例为已经接受了6~12个月抗凝治疗的患者, 分别接受利伐沙班602例或安慰剂594例治疗, 结果利伐沙班组较安慰剂组显著降低了血栓栓塞复发事件发生率(1.3%比7.1%, 危险比0.18, 95%CI 0.09%~0.29%), 利伐沙班组有4例发生非致命性出血事件。作为最早完成VTE预防和治疗的新型抗凝药物, 利伐沙班也被第9版ACCP指南列入推荐用药。截止到2012年9月, 利伐沙班用于骨科手术后预防的适应证在欧盟、美国、中国等120个国家获得批准上市, 其用于治疗DVT/PE的适应证已经获得美国和欧盟等63个国家批准上市。
通过上述3种药物临床试验结果, 可以发现目前这3种口服抗凝药物在安全性和有效性方面均不劣于传统低分子肝素+VKA治疗; 但是否能得出优于后者的结果, 还需要慎重看待。
其他类型抗凝药物
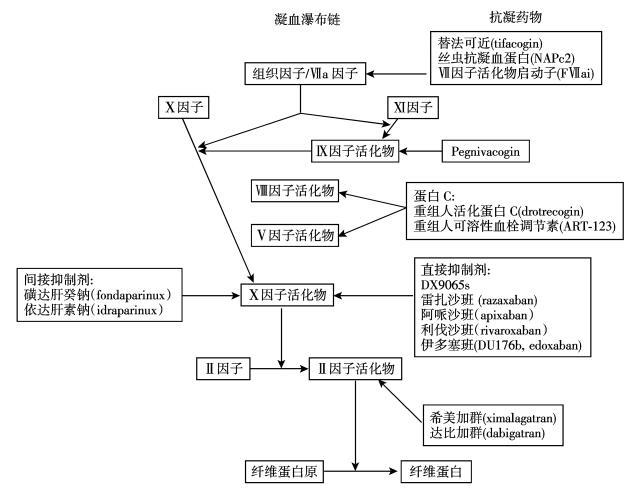
除了上述3种药物, 实际上还有不少其他类型作用于不同靶点的在研新抗凝药物(图 1)[29], 其中有几个药物也值得关注。
磺达肝癸钠, 为1种合成的低分子肝素的核心——戊聚糖, 是Ⅹa因子间接抑制剂。其作为VTE预防药物已经在包括中国在内的多个国家上市, 作为VTE治疗药物也已在欧洲上市。
DU-176b, 也是1种Ⅹa因子直接抑制剂, 其化学名为伊多塞班(edoxaban), 已开始用于VTE治疗的3期临床试验, 在2012年9月完成全部入组患者的招募。
Betrixaban, 同样也是1种Ⅹa因子直接抑制剂, 用于骨关节术后VTE预防的2期试验已经完成。
AVE-5026, 1种超低分子肝素, 相对分子质量平均为2000~3000, 是由普通肝素提取而成的, 目前已经完成2期试验, 进入3期临床试验。
一般认为, 未来新抗凝药物应该具有以下几个主要特征:(1)易于使用; (2)作用位点尽量单一, 作用方式可以为直接或间接作用; (3)特异性强; (4)使用途径尽量以口服为宜; (5)药代动力学方面, 应该起效快, 停药后的后续效果时间短; (6)与其他药物相互作用少; (7)实验室监测要求低; (8)出血、肝肾功能损害等不良反应少; (9)有特异性或非特异性抗体拮抗, 以便及时治疗出血等不良反应。
在研究这些药物的特点时, 还需要注意以下几个问题。
是Ⅹa还是Ⅱa因子抑制剂:组织因子(Ⅶ因子)激活Ⅹa因子聚集, 从而启动了整个凝血系统的反应瀑布, 即正是Ⅹa因子的启动和激活, 使得凝血酶(Ⅱa因子)形成凝血酶复合物, 最终形成血栓。所以, 一直以来, 学术界有争论, 究竟应该选择Ⅹa因子抑制剂, 还是选择Ⅱa因子抑制剂更为安全有效。有少量动物学研究发现, Ⅹa因子抑制剂可能比Ⅱa因子抑制剂出血风险减少。但这个结论又会带来另一个问题, 即如何平衡抑制血栓和减少出血之间的风险/收益比。另外, 药物的使用时间和剂量本身也会与治疗的安全性和有效性相关。
另外, 一旦药物选择凝血因子单一靶点, 还需要明确这种药物与作用靶点的结合是可逆的还是不可逆的, 有效简便的拮抗药物也是保证药物安全的必要条件。
新药物监测:临床药物研究, 在药代动力学和药效动力学研究后, 还需在动物的动脉和静脉血栓模型中验证其药物出血风险及其他不良反应。
对于严格控制入排标准进行的药物试验, 很难有效地观察药物的有效性以及对于不同剂量的耐受性。实际上, 常见实验室监测指标均无法用于新药物监测, 以评估出血风险。磺达肝癸钠(fondaparinux)和依达肝素钠(idraparinux)这两种凝血酶依赖特异性Ⅹa因子抑制剂, 并不影响凝血酶原时间(prothrombin time, PT)和活化部分凝血酶原时间(activated partial thromboplastin time, APTT), 即使使用超高剂量导致了出血事件, 监测指标也不会出现改变[30]。
一些新的药物, 如利伐沙班、DU-176b、美拉加群(melagatran)、达比加群(dabigatran)等可能会导致PT时间延长, 但是这种延长无法用INR监测。目前看来, INR只能用于华法林监测, 因为VKA阻断了多个凝血因子的合成。
另外, 还需要理解为什么各种含有抗Ⅹa因子活性的药物实验室检查值完全不同, 如PT。以上提到磺达肝癸钠并不会延长PT, 因为其对游离Ⅹa因子的作用很小。相反, Ⅹa因子直接抑制剂, 如利伐沙班会延长PT, 因为其对游离Ⅹa因子和Ⅹa因子与磷脂的复合物都有相同的作用。一些新的药物有共同的作用靶点, 如特异性Ⅹa因子和Ⅱa因子抑制剂, 它们对PT或APTT的影响并不相同。除了它们与游离Ⅹa因子和Ⅹa因子复合物结合力不同外, 药物与血栓结合的Ⅹa因子的结合也有不同, 如Ⅹa因子直接抑制剂(利伐沙班和阿哌沙班)可以抑制各种形态下的Ⅹa因子, 而间接Ⅹa因子抑制剂则主要与游离的Ⅹa因子作用。
药物给药途径:口服给药途径是最佳途径, 尤其对VKA替代产品而言。为此还需要了解药物在体内的吸收、生物利用度以及与伴随食物吸收时的相互作用。目前已经知道, 肝功能评价是安全性评价的必要指标, 尤其对希美加群更是如此。由于希美加群有较明显的肝功能损害作用, 已经在欧洲被召回, 美国FDA也已拒绝了其上市申请。
药物治疗窗:药物治疗窗也是研究重点, 如达比加群, 其药物剂量与血栓发生事件有显著的相关性; 相反, 利伐沙班药物筛选研究发现, 其剂量相差12倍, 与血栓发生事件无显著相关性。
结论
VTE治疗和预防新抗凝药物已经进入飞速发展的新阶段, 多个药物, 尤其是阿哌沙班、达比加群和利伐沙班大规模3期临床试验结果令人鼓舞。我们有理由期待它们在不远的将来, 对肝素+华法林, 这个传统的VTE抗凝治疗方案发出强有力的挑战。
-
[1] Heit JA. The epidemiology of venous thromboembolism in the community[J]. Arterioscler Thromb Vasc Biol, 2008, 28:370-372. DOI: 10.1161/ATVBAHA.108.162545
[2] Schünemann HJ, Cook D, Guyatt G, et al.Methodology for antithrombotic and thrombolytic therapy guideline development:American College of Chest Physicians evidence-based clinical practice guidelines (8th ed)[J]. Chest, 2008, 133:113S-122S. DOI: 10.1378/chest.08-0666
[3] Guyatt GH, Eikelboom JW, Gould MK, et al. Approach to outcome measurement in the prevention of thrombosis in surgical and medical patients:antithrombotic therapy and prevention of thrombosis, 9th ed:American College of Chest Physicians evidence-based clinical practice guidelines[J]. Chest, 2012, 141(2 Suppl):e185S-194S. http://www.onacademic.com/detail/journal_1000038942250310_d3e0.html
[4] 吕厚山, 徐斌.人工关节置换术后下肢深静脉血栓形成[J].中华骨科杂志, 1999, 19:155-156. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zhgkzz98199903008 [5] 孙建行.创伤性下肢深静脉血栓形成的治疗探讨[J].中国中医骨伤科杂志, 2007, 15:6-8. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgzygsk200704002 [6] 中华医学会心血管病学分会肺血管病学组, 中国医师协会心血管内科医师分会.急性肺血栓栓塞症诊断治疗中国专家共识[J].中华内科杂志, 2010, 49:74-81. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zhnk201001026 [7] 中华医学会外科学分会血管外科学组.深静脉血栓形成的诊断和治疗指南(第二版)[J].中华外科杂志, 2012, 50:611-613. http://qikan.cqvip.com/Qikan/Article/Detail?id=1003027731 [8] Raghavan N, Frost CE, Yu Z, et al. Apixaban metabolism and pharmacokinetics after oral administration to humans[J]. Drug Metab Dispos, 2009, 37:74-81. DOI: 10.1124/dmd.108.023143
[9] Pinto DJ, Orwat MJ, Koch S, et al. Discovery of 1-(4-methoxyphenyl)-7-oxo-6-(4-(2-oxopiperidin-1-yl)phenyl)-4, 5, 6, 7-tetrahydro-1H-pyrazolo[3, 4-c]pyridine-3-carboxamide (apixaban, BMS-562247), a highly potent, selective, efficacious, and orally bioavailable inhibitor of blood coagulation factor Ⅹa[J]. J Med Chem, 2007, 50:5339-5356. DOI: 10.1021/jm070245n
[10] Buller H, Deitchman D, Prins M, et al.Efficacy and safety of the oral direct factor Ⅹa inhibitor apixaban for symptoma-tic deep vein thrombosis:the Botticelli DVT dose-ranging study[J]. J Thromb Haemost, 2008, 6:1313-1318. DOI: 10.1111/j.1538-7836.2008.03054.x
[11] Lassen MR, Raskob GE, Gallus A, et al. Apixaban or enoxaparin for thromboprophylaxis after knee replacement[J]. N Engl J Med, 2009, 361:594-604. DOI: 10.1056/NEJMoa0810773
[12] Lassen MR, Raskob GE, Gallus A, et al. ADVANCE-2 investigators. Apixaban versus enoxaparin for thromboprophylaxis after knee replacement (ADVANCE-2):a randomised double-blind trial[J]. Lancet, 2010, 375:807-815. DOI: 10.1016/S0140-6736(09)62125-5
[13] Falck-Ytter Y, Francis CW, Johanson NA, et al. Prevention of VTE in orthopedic surgery patients:antithrombotic therapy and prevention of thrombosis, 9th ed:American College of Chest Physicians evidence-based clinical practice guidelines[J]. Chest, 2012, 141(2 Suppl):e278S-325S. http://cid.oxfordjournals.org/external-ref?access_num=10.1378/chest.11-2296&link_type=DOI
[14] Blech S, Ebner T, Ludwig-Schwellinger E, et al. The metabolism and disposition of the oral direct thrombin inhibitor, dabigatran, in humans[J]. Drug Metab Dispos, 2008, 36:386-399. DOI: 10.1124/dmd.107.019083
[15] Eriksson BI, Dahl OE, Rosencher N, et al. Dabigatran etexilate versus enoxaparin for prevention of venous thromboembolism after total hip replacement:a randomised, double-blind, non-inferiority trial[J]. Lancet, 2007, 370:949-956. DOI: 10.1016/S0140-6736(07)61445-7
[16] Eriksson BI, Dahl OE, Rosencher N, et al. Oral dabigatran etexilate vs. subcutaneous enoxaparin for the prevention of venous thromboembolism after total knee replacement:the RE-MODEL randomized trial[J]. J Thromb Haemost, 2007, 5:2178-2185. DOI: 10.1111/j.1538-7836.2007.02748.x
[17] Ginsberg JS, Davidson BL, Comp PC, et al. Oral thrombin inhibitor dabigatran etexilate vs. North American enoxaparin regimen for prevention of venous thromboembolism after knee arthroplasty surgery[J]. J Arthroplasty, 2009, 24:1-9. DOI: 10.1016/S0883-5403(08)00834-6
[18] Schulman S, Kearon C, Kakkar AK, et al. Dabigatran versus warfarin in the treatment of acute venous thromboembolism[J]. N Engl J Med, 2009, 361:2342-2352. http://gut.bmj.com/external-ref?access_num=10.1056/NEJMoa0906598&link_type=DOI
[19] Schulman S, Kakkar AK, Schellong S, et al.A randomized trial of dabigatran versus warfarin in the treatment of acute venous thromboembolism (RECOVER Ⅱ)[J]. Blood, 2011, 118:205.
[20] Schulman S, Baanstra D, Eriksson H, et al.Dabigatran vs. placebo for extended maintenance therapy of venous thromboembolism[J]. J Thromb Haemost, 2011, 9:22. http://www.researchgate.net/publication/295663864_Dabigatran_vs_placebo_for_extended_maintenance_therapy_of_venous_thromboembolism
[21] Kubitza D, Becka M, Wensing G, et al.Safety, pharmacodynamics, and pharmacokinetics of BAY 59-7939-an oral, direct Factor Ⅹa inhibitor-after multiple dosing in healthy male subjects[J]. Eur J Clin Pharmacol, 2005, 61:873-880. DOI: 10.1007/s00228-005-0043-5
[22] Eriksson BI, Borris LC, Friedman RJ, et al. Rivaroxaban versus enoxaparin for thromboprophylaxis after hip arthroplasty[J]. N Engl J Med, 2008, 358:2765-2775. DOI: 10.1056/NEJMoa0800374
[23] Kakkar AK, Brenner B, Dahl OE, et al. Extended duration rivaroxaban versus short-term enoxaparin for the prevention of venous thromboembolism after total hip arthroplasty:a double-blind, randomised controlled trial[J]. Lancet, 2008, 372:31-39. DOI: 10.1016/S0140-6736(08)60880-6
[24] Turpie AG, Lassen MR, Davidson BL, et al. Rivaroxaban versus enoxaparin for thromboprophylaxis after total knee arthroplasty (RECORD4):a randomised trial[J]. Lancet, 2009, 373:1673-1680. DOI: 10.1016/S0140-6736(09)60734-0
[25] Lassen MR, Ageno W, Borris LC, et al. Rivaroxaban versus enoxaparin for thromboprophylaxis after total knee arthroplasty[J]. N Engl J Med, 2008, 358:2776-2786. DOI: 10.1056/NEJMoa076016
[26] EINSTEIN Investigators, Bauersachs R, Berkowitz SD, et al. Oral rivaroxaban for symptomatic venous thromboembolism[J]. N Engl J Med, 2010, 363:2499-2510. DOI: 10.1056/NEJMoa1007903
[27] EINSTEIN-PE Investigators, Büller HR, Prins MH, et al. Oral rivaroxaban for the treatment of symptomatic pulmonary embolism[J].N Engl J Med, 2012, 366:1287-1297. DOI: 10.1056/NEJMoa1113572
[28] Romualdi E, Donadini MP, Ageno W. Oral rivaroxaban after symptomatic venous thromboembolism:the continued treatment study (EINSTEIN-extension study)[J]. Expert Rev Cardiovasc Ther, 2011, 9:841-844. DOI: 10.1586/erc.11.62
[29] Weitz JI, Bates SM. New anticoagulants[J]. J Thromb Haemost, 2005, 3:1843-1853. DOI: 10.1111/j.1538-7836.2005.01374.x
[30] Samama MM, Le Flem L, Guinet C, et al. Comparative responses of some clotting assays to fondaparinux, dabigatran and rivaroxaban. 20th international congress on thrombosis, June 25-28, 2008[C]. Athens, Greece: [s.n.], 2008.
-
期刊类型引用(5)
1. 罗丹,王璞. 静脉血栓栓塞症的抗凝现状及新型抗凝药的研究进展. 现代医药卫生. 2017(21): 3294-3296 .  百度学术
百度学术
2. 杜兴升,喻长纯. 骨科围术期静脉血栓栓塞症的病因及诊疗分析. 世界最新医学信息文摘. 2016(08): 108+111 .  百度学术
百度学术
3. 户海宁. 内科住院患者静脉血栓栓塞症的临床防治. 大众科技. 2015(01): 112-114 .  百度学术
百度学术
4. 陈洪,陈虹. 肺血栓栓塞症治疗的研究进展. 临床肺科杂志. 2014(02): 331-334 .  百度学术
百度学术
5. 卢朝黎,李宇星. 下肢创伤患者术后应用利伐沙班预防静脉血栓栓塞症的疗效及安全性. 实用药物与临床. 2014(08): 1019-1022 .  百度学术
百度学术
其他类型引用(3)

 作者投稿
作者投稿 专家审稿
专家审稿 编辑办公
编辑办公 邮件订阅
邮件订阅 RSS
RSS

 下载:
下载:











